News
Proof-of-Concept-Förderung des ERC für 'Design2Guide': Neue Designstrategie für experimentelle Modelle von Tumorgeweben
for English text please scroll down
Forscher:innen des Leibniz-Instituts für Polymerforschung Dresden nutzen eine Hydrogel-basierte Plattform, um eine rationale Designstrategie für Modelle von Tumorgeweben zu entwickeln und bessere Therapieoptionen für Menschen mit Bauchspeicheldrüsenkrebs zu finden. Um die Forschung voranzutreiben, erhielt das interdisziplinäre Team von Professorin Daniela Lössner vom Europäischen Forschungsrat (ERC) jetzt eine Proof-of-Concept-Förderung für das Projekt 'Design2Guide: Cell-instructive matrices to deconstruct tumour tissues'.
Die Forschung des Teams geht ein klinisches Problem mit einem innovativen Ansatz an. Bauchspeicheldrüsenkrebs ist eine der tödlichsten Krebsarten und nur 10 % der Menschen, bei denen diese Krankheit diagnostiziert wird, überleben fünf Jahre nach der Diagnose. Um bessere Therapien zu finden, werden patientenspezifische Modelle entwickelt, die die Biologie des Tumorgewebes und Wechselwirkungen zwischen verschiedenen Zelltypen nachahmen. Ziel von 'Design2Guide' ist es, eine steuerbare Plattform für experimentelle Studien an der menschlichen Krankheit im Labor zu schaffen. Die neue Plattform soll dazu dienen, bessere Behandlungsmöglichkeiten für die Krankheit zu finden.
Die schlechte Prognose bei Bauchspeicheldrüsenkrebs hängt u.a. damit zusammen, dass die Tumore von fibrotischem Gewebe und einer extrazellulären Kollagenmatrix umgeben sind. Matrixproteine regulieren wichtige Zellfunktionen. Mit verfügbaren experimentellen Modellen können das fibrotische Gewebe und die Matrix dieser Krankheit nicht nachgebildet werden. Mehrere Studien, darunter zwei des Teams von Daniela Lössner (Advanced Healthcare Materials 2022 doi:10.1002/adhm.202201907, Nature Communications 2021 doi:10.1038/s41467-021-25921-9), haben die Schlüsselrolle von einzelnen Matrix-Komponenten bei der Steuerung von Zellfunktionen aufgezeigt und betonen die Notwendigkeit, Hydrogel-basierte Systeme zu entwickeln.
Das Problem
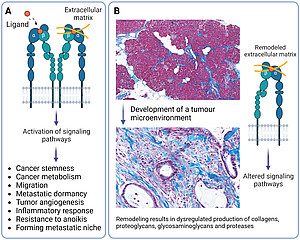
Die extrazelluläre Matrix von Bauchspeicheldrüsenkrebs ist sehr komplex und besteht aus vielen fibrotischen Proteinen, darunter Kollagene, Proteoglykane, Laminine und Fibronektin. In Tumorgeweben stimuliert der Umbau der Matrix das Wachstum von Krebszellen, die ihrerseits über Integrine, eine wichtige Klasse von Zelloberflächen- und Adhäsionsrezeptoren, mit der Matrix interagieren (Abbildung 1A). Integrine erleichtern die Zell-Zell- und Zell-Matrix-Interaktionen in der Umgebung des Tumors und steuern Signalwege, die zum Fortschreiten der Krankheit und zur Metastasierung führen (Abbildung 1B). Daher sind Integrine zu einem wichtigen Gegenstand der Forschung an neuen Therapien geworden, die in klinischen Studien getestet werden. Allerdings fehlt trotz der bedeutenden Rolle der Zelladhäsion ein robuster technischer Ansatz, um das spezifische Adhäsionsprofil von Krebszellen nachzuahmen und das krankheitsrelevante Integrinprofil in experimentellen Modellen zu untersuchen.
Die Lösung
'Design2Guide' schlägt eine rationale Designstrategie für ein krankheitsrelevantes 3D-Krebsmodell vor, die auf zwei grundlegenden Aspekten beruht: Erstens einer minimalistischen synthetischen Matrix, die individuelle Matrixkomponenten von Tumorgeweben in Form von Polyethylenglycol-Hydrogelen enthält, und zweitens der Fähigkeit, Integrinprofile zu steuern und anschließend Signalwege zu aktivieren. Die 'Design2Guide'-Plattform zielt auf die Entwicklung Hydrogel-basierter Systeme zur Nachahmung von Tumorgewebe ab, um die Zell-Zell- und Zell-Matrix-Interaktionen bei Menschen mit Bauchspeicheldrüsenkrebs zu untersuchen. Die Forschung wird Wissenschaftler:innen auf dem Gebiet des Engineering von Tumorgewebe zugutekommen. Dieses neue, interdisziplinäre Forschungsgebiet verbindet Tissue Engineering und Zellbiologie (Nature Reviews Materials 2023 doi:10.1038/s41578-023-00535-3).
Kontakt
Prof. Dr. Daniela Lössner
loessner@ipfdd.de
------------------------------
Researchers at the Leibniz Institute of Polymer Research Dresden are using a hydrogel-based model to develop a rational design strategy and guide better therapeutic options for people diagnosed with pancreatic cancer. Therefore, the interdisciplinary team of Professor Daniela Lössner received a Proof-of-Concept grant ‘Design2Guide’ from the European Research Council (ERC).
The team’s research addresses a clinical problem with an innovative approach. Pancreatic cancer is one of the deadliest cancers and only 10% of people diagnosed with this disease survive 5 years after diagnosis. To find better therapies, patient-specific models that mimic the biology of tumour tissues and interactions between different cell types are developed. The aim of ‘Design2Guide’ is to build a controllable platform for studying the human disease in the laboratory. The new platform will be used to discover better ways of treating the disease.
Pancreatic cancer has a fibrotic, or scar-like, tumour microenvironment and a collagenous extracellular matrix, which correlate with poor prognosis and patient survival. Important cell functions are associated with the presence of several matrix proteins. Current experimental models fail to replicate the specific microenvironment and matrix of this disease. Several studies, including two studies from Daniela Lössner’s team (Advanced Healthcare Materials 2022 doi:10.1002/adhm.202201907, Nature Communications 2021 doi:10.1038/s41467-021-25921-9), highlight the key role of specific matrix components in driving cell functions, emphasizing the need to design cell-instructive matrices.
The problem
The extracellular matrix of pancreatic cancer is very complex and consists of many fibrotic proteins, including collagens, proteoglycans, laminins and fibronectin. In tumour tissues, the remodelling of the matrix induces the growth of cancer cells, which in turn interact with the matrix through integrins, a major class of cell surface and adhesion receptors (Figure 1A). Integrins facilitate cell-cell and cell-matrix interactions in the tumour microenvironment and guide signalling pathways, leading to disease progression and metastasis (Figure 1B). Thus, integrins have become an important target for anti-cancer therapeutics, which are tested in clinical trials. Despite the critical role of the adhesion requirements in guiding cell behaviour, a robust engineering approach to mimic the specific adhesion profile of cancer cells and instruct the disease-relevant integrin profile in experimental models is missing.
The solution
‘Design2Guide’ proposes a rational design strategy of a disease-relevant 3D cancer model based on two fundamental aspects: firstly, a minimalistic synthetic matrix that incorporates essential matrix components of tumour tissues in the form of polyethylene glycol hydrogels, and secondly, the capacity to instruct integrin profiles and subsequently activate signalling pathways. The ‘Design2Guide’ platform addresses the need for developing cell-instructive matrices to deconstruct tumour tissues in order to studying the cell-cell and cell-matrix interactions present in people diagnosed with pancreatic cancer. The research will benefit scientists in the field of tumour tissue engineering, an interdisciplinary research area combining tissue engineering and cell biology (Nature Reviews Materials 2023 doi:10.1038/s41578-023-00535-3). The long-term impact of the new platform will be a generalized approach for targeting tissue-level adhesion requirements in synthetic matrices, enabling new knowledge about how to treat solid tumours.
Contact
Prof. Daniela Loessner
loessner@ipfdd.de
01.08.2023

